Μεσογειακή αναιμία: Διάγνωση παθολογικού εμβρύου πριν την έναρξη της εγκυμοσύνης με τη βοήθεια των ακτίνων laser.
Οι εξελίξεις στον χώρο της σύγχρονης μαιευτικής παρακολούθησης με την υψηλή ποιότητα της ιατρικής φροντίδας κατά την εγκυμοσύνη και τον τοκετό δίνουν σήμερα την δυνατότητα στις γυναίκες να αποκτήσουν ένα υγιές παιδί. Η απόκτηση ενός φυσιολογικού παιδιού είναι απαίτηση όλων των ζευγαριών που σχεδιάζουν μία οικογένεια.
Παρ’ όλα αυτά, 1% των παιδιών που γεννιούνται πάσχουν από μία κληρονομική γενετική νόσο. Με την κλασική προγεννητική διάγνωση, υπάρχει η δυνατότητα να ελέγξουμε ένα έμβρυο υψηλού κινδύνου για συγκεκριμένη γενετική νόσο, με διάφορες τεχνικές, όπως με βιοψία χοριονικών λαχνών ή αμνιοκέντηση στο τέλος του πρώτου ή αρχή του δευτέρου τριμήνου της εγκυμοσύνης.
Η διάγνωση γίνεται με κυτταρογενετικές, βιοχημικές ή μοριακές μεθόδους ανάλυσης, ανάλογα με την πάθηση για την οποία το έμβρυο είναι σε υψηλό κίνδυνο. Αν βρεθεί ότι το έμβρυο πάσχει από κάποια ασθένεια, το ζευγάρι έχει την δυνατότητα διακοπής της εγκυμοσύνης, όμως αυτό συνεπάγεται οργανικό και ψυχολογικό κόστος.
Η πιθανότητα μετάδοσης μιας γενετικής νόσου από ζευγάρια που είναι φορείς προς τους απογόνους είναι πολύ μεγάλη. Η διάγνωση μιας γενετικής νόσου από ζευγάρια φορείς, έχει σαν αποτέλεσμα την διακοπή της εγκυμοσύνης και σε ορισμένες γυναίκες επανειλημμένες διακοπές εγκυμοσύνης.
Εναλλακτική λύση στην προγεννητική διάγνωση για την αποφυγή πιθανής διακοπής της κυήσεως αποτελεί η εφαρμογή μίας καινούργιας τεχνικής, η προεμφυτευτική διάγνωση. Κατά τη μέθοδο αυτή γίνεται η ανίχνευση του γονοτύπου των εμβρύων πριν την αρχή της εγκυμοσύνης με τη βοήθεια της εξωσωματικής γονιμοποίησης.
Η προεμφυτευτική διάγνωση δηλαδή επιτρέπει την ανίχνευση του γενετικού υλικού των εμβρύων πριν από την εμφύτευσή τους στην μήτρα. Η μέθοδος της προεμφυτευτικής διάγνωσης αποτελεί συνδυασμό της εξωσωματικής γονιμοποίησης και ειδικών διαγνωστικών τεχνικών γενετικής ανάλυσης.
Η προεμφυτευτική γενετική διάγνωση γίνεται κατά την διάρκεια ενός κύκλου εξωσωματικής γονιμοποίησης, και παρεμβάλλεται στο διάστημα ανάμεσα στην γονιμοποίηση και την εμβρυομεταφορά. Όπως σε κάθε κύκλο εξωσωματικής γονιμοποίησης, γίνεται φαρμακευτική διέγερση των ωοθηκών της γυναίκας, ακολουθεί η διακολπική λήψη των ωαρίων με υπερηχογραφική καθοδήγηση και η γονιμοποίηση τους στο εργαστήριο με το σπέρμα του συζύγου, ενώ η καλλιέργεια των γονιμοποιημένων ωαρίων συνεχίζεται για τρεις μέρες.
Την τρίτη μέρα της καλλιέργειας,τα γονιμοποιημένα ωάρια που βρίσκονται στο στάδιο των έξι με δέκα κυττάρων, υποβάλλονται σε βιοψία, όπου γίνεται η λήψη ενός κυττάρου (βλαστομεριδίου). Στο στάδιο αυτό της ανάπτυξης του γονιμοποιημένου ωαρίου (στάδιο αυλάκωσης), όπου γίνεται η βιοψία, το καθ ένα από τα κύτταρά του παραμένει πολυδύναμο, δηλαδή από μόνο του θα μπορούσε να δώσει γένεση σε όλους τους ιστούς του εμβρύου. Έτσι κατά την αφαίρεση ενός κυττάρου δεν υφίσταται βλάβη στο έμβρυο. Η ασφάλεια της βιοψίας έχει μελετηθεί εκτενώς σε μεγάλα κέντρα σε όλο τον κόσμο.
Το κύτταρο που αφαιρείται από κάθε γονιμοποιημένο ωάριο υποβάλλεται σε γενετική ανάλυση ενώ η καλλιέργεια των γονιμοποιημένων ωαρίων συνεχίζεται στο εργαστήριο μέχρι το στάδιο της βλαστοκύστης.
(Βλαστοκύστη ονομάζουμε το γονιμοποιημένο ωάριο κατά την 6η μέρα μετά την γονιμοποίηση, όταν δηλαδή αποτελείται πλέον από 140 με 200 κύτταρα). Η γενετική διάγνωση θα υποδείξει ποια βλαστοκύστη θα μεταφερθεί στην μήτρα, αποκλείοντας εκείνες που φέρουν γενετικές ασθένειες.
Η πιθανότητα εγκυμοσύνης κατά την μεταφορά βλαστοκύστεων στην μήτρα ξεπερνάει το κλασικό ποσοστό επιτυχίας της εξωσωματικής γονιμοποίησης γιατί σ αυτή την χρονική στιγμή υπάρχει ο ιδανικός συγχρονισμός τους με το ενδομήτριο, όπως ακριβώς γίνεται κατά την φυσική σύλληψη. Πράγματι, κατά την φυσική σύλληψη, είναι γνωστό ότι η έναρξη της εγκυμοσύνης γίνεται κατά την 6η μέρα μετά την γονιμοποίηση, όταν δηλαδή τα γονιμοποιημένα ωάρια ολοκληρώσουν το ταξίδι τους από την σάλπιγγα προς την κοιλότητα της μήτρας.
Πιο συγκεκριμένα, η λήψη του κυττάρου από το γονιμοποιημένο ωάριο στο στάδιο 3ων ημερών γίνεται στο εργαστήριο με τη χρήση ειδικού λέιζερ που κατευθύνεται με τη βοήθεια μικροσκοπίου. Οι ακτίνες λέιζερ δημιουργούν μια τομή ακριβείας στο περίβλημα του γονιμοποιημένου ωαρίου έτσι ώστε να δημιουργηθεί μία οπή.
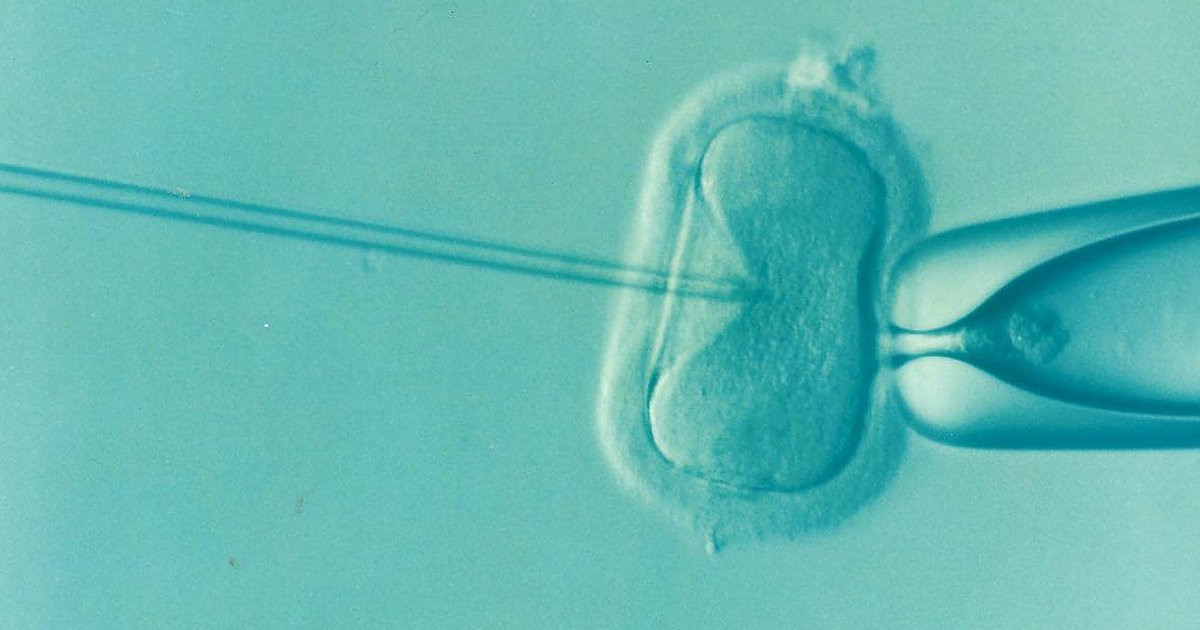
Εικόνα 1: Λήψη ενός κυττάρου από γονιμοποιημένο ωάριο τρεις μέρες μετά την γονιμοποίηση
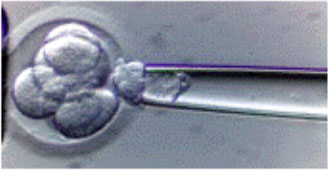
Με τον τρόπο αυτό αναρροφάται με την βοήθεια μικροπιπέτας ένα κύτταρο (Εικόνα 1), το οποίο θα χρησιμεύσει για την διάγνωση. Σε αντίθεση με τις παλαιότερες τεχνικές που χρησιμοποιούν χημικά μέσα προκειμένου να γίνει η διάνοιξη της οπής στο περίβλημα του γονιμοποιημένου ωαρίου, οι ακτίνες λέιζερ προσφέρουν ακρίβεια και ελαχιστοποίηση της βλάβης που θα μπορούσε να υποστούν τόσο τα κύτταρα του γονιμοποιημένου ωαρίου, όσο και του κυττάρου που αφαιρείται.
Η γενετική ανάλυση όπως είναι εύκολα αντιληπτό θα πρέπει να γίνει χρησιμοποιώντας ένα μόνο κύτταρο από κάθε γονιμοποιημένο ωάριο και αυτό δικαιολογεί την δυσκολία και την ευαισθησία της διάγνωσης, που παρ’ όλα αυτά έχει ένα υψηλό ποσοστό αξιοπιστίας.
Πρόσφατα εφαρμόζεται η βιοψία στο στάδιο της βλαστοκύστης, μία νέα τεχνική βιοψίας στα γονιμοποιημένα ωάρια, που δίνει την δυνατότητα αφαίρεσης περισσοτέρων κυττάρων για γενετική ανάλυση. Μετά την διάγνωση, η μεταφορά των βλαστοκύστεων στην μήτρα, γίνεται την ίδια μέρα.
Πιο συγκεκριμένα, η βλαστοκύστη αποτελείται από διαφοροποιημένα κύτταρα δύο ειδών (βλ. Εικόνα 2).
Τα τροφοδερμικά κύτταρα (ή κύτταρα τροφοβλάστης) που μετά την εμφύτευση δημιουργούν τον πλακούντα και τα κύτταρα του εμβρυϊκού πόλου (ή κύτταρα εμβρυοβλάστης) που μετά την εμφύτευση δημιουργούν το έμβρυο.
Εικόνα 2
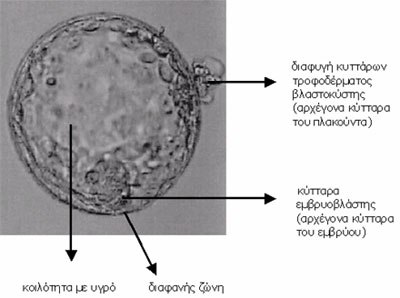
Με την βοήθεια των ακτίνων λέιζερ γίνεται λήψη τροφοδερμικών κυττάρων από τη βλαστοκύστη με μία απλή διαδικασία κατά την οποία δημιουργείται ένα μικρό άνοιγμα της διαφανούς ζώνης, προκαλώντας έτσι την πρόσκαιρη διαφυγή μερικών κυττάρων τροφοβλάστης. Τα κύτταρα αυτά αφαιρούνται και υποβάλλονται σε γενετική ανάλυση με αποτέλεσμα η διάγνωση να γίνεται ευκολότερα και με μεγαλύτερη αξιοπιστία.
Στην ουσία πρόκειται για γενετική ανάλυση ανάλογη με εκείνη που γίνεται κατά την λήψη τροφοβλάστης από το έμβρυο μόνο που στην περίπτωση αυτή η εγκυμοσύνη δεν έχει ακόμη ξεκινήσει. Η διάγνωση προηγείται της εγκυμοσύνης και δεν έπεται – όπως στην περίπτωση της τροφοβλάστης με ότι αυτό συνεπάγεται.
Ανεξάρτητα από την χρονική στιγμή λήψης των κυττάρων (3η ή 6η μέρα μετά την γονιμοποίηση) εφαρμόζονται διαγνωστικές τεχνικές για την ανάλυση των χρωμοσωμάτων ή για την μοριακή ανάλυση DNA, ανάλογα με την πάθηση για την οποία το έμβρυο βρίσκεται σε υψηλό κίνδυνο.
Οι τεχνικές που εφαρμόζονται είναι υψηλής ακρίβειας και ευαισθησίας, όπως η αλυσιδωτή αντίδραση της πολυμεράσης (Polymerase Chain Reaction – PCR) που επιτρέπει τον πολλαπλασιασμο ενός προεπιλεγμένου τμήματος DNA μέχρι και 1.000.000 φορές ή υβριδισμός in situ (FISH= Fluorescent In Situ Hybridisation).
Οι ανωτέρω γενετικές τεχνικές εφαρμόζονται για την διάγνωση πολλών κληρονομικά μεταδιδομένων ασθενειών, γονιδιακών (β-θαλασσαιμία) και φυλοσύνδετων στο χρωμόσωμα Χ (αιμορροφιλία, μυϊκή δυστροφία Duchenne, αμαυροειδή αμφιβληστροειδοπάθεια – Retinitis Pigmentosa).
Για την Ελλάδα το πιο συχνό και μείζονος βαρύτητας μονογονιδιακό νόσημα είναι τα μεσογειακά σύνδρομα (10% του πληθυσμού είναι φορείς β μεσογειακής αναιμίας και άλλων σχετιζομένων αιμοσφαιρινοπαθειών) τα οποία παρουσιάζουν μεγάλη φαινοτυπική και κλινική ετερογένεια (περισσότερες από 20 διαφορετικές σημειακές μεταλλάξεις στο β γονίδιο αιμοσφαιρίνης).
Ανά τον κόσμο, τα τελευταία 10 χρόνια, έχουν γίνει περίπου 2,000 κύκλοι εξωσωματικής γονιμοποίησης και περισσότερα από 250 υγιή βρέφη έχουν γεννηθεί. Στην Ελλάδα έχουν γίνει 80 κύκλοι εξωσωματικής γονιμοποίησης και έχουν γεννηθεί 21 παιδιά και βρίσκονται 4 εγκυμοσύνες σε εξέλιξη.
(Σε συνεργασία με: Γεωργία Κόκκαλη, BSc., Msc Κλινικός Εμβρυολόγος Κέντρο Ανθρώπινης Αναπαραγωγής)
Διαβάστε επίσης
- Αν σκέφτεστε να μείνετε έγκυος…
- Τερηδόνα και ουλίτιδα της κύησης
- Εγκυμοσύνη και ερυθρά
- Θυμόμαστε το προφυλακτικό όλο το χρόνο κι όχι μόνο στις 13 Φεβρουαρίου
- Σακχαρώδης διαβήτης κύησης: η σωστή παρακολούθηση πρέπει να ξεκινά από νωρίς
Ο γυναικολόγος Κωνσταντίνος Πάντος έλαβε το πτυχίο της ιατρικής από το Πανεπιστήμιο Αθηνών το 1981. Ειδικεύτηκε στη Μαιευτική – Γυναικολογία στο Πανεπιστήμιο Αθηνών και το 1988 του απονεμήθηκε ο τίτλος του Διδάκτορα της Ιατρικής Σχολής του Πανεπιστημίου Αθηνών. Εξειδικεύτηκε στον τομέα της ιατρικώς υποβοηθούμενης αναπαραγωγής στο Βασιλικό Νοσοκομείο Μελβούρνης στην Αυστραλία (1987-1989). Το 1994, ο Δρ Πάντος ίδρυσε το Κέντρο Ανθρώπινης Αναπαραγωγής.